文献速递 | 礼来开发的半自动化两步抗体纯化工艺
发布公告时光:2022-05-23预览频率:次 赛分新闻
渐渐抵抗能力工艺创新工艺进一步,尤其是是人源化小鼠和噬菌体/鲜酵母库的方式的会出现,就可以发展出大量的各不相同类型的的抵抗能力样件英文,只为可如何快速的淘汰开立有可发展深入分析特点的样件英文,对待如何快速的、高效益化学合成高溶解度样件英文提交高让。
杏彩体育网
创新客人礼来(Eli Lilly and Company)在《MABS》杂质发过名为《Development of a robust and semi-automated two-step antibody purification process》篇文章,文章分为亲和层析及表面积排阻化学合成柱 SRT-10C SEC-300构建高速、高效、性价比最高提取高溶解度抗体阳性的办法,云同步处理好内毒性清楚难题,很大升高纯化速度,有益于高速推进项目建设调查任务管理器。
背景介绍
免疫免疫免疫抗体产品的发掘建设技術掣肘正在逐步被揍破,真对一个靶点可以的发掘建设成百上百万的免疫免疫免疫抗体大碳原子结构,相对 该大碳原子结构为什么要成药可以制法一些量的样机实现迅速的筛分,从而评价指标其可的发掘建设性(developability)各类制作工艺可实施性(manufacturability)。就此,采用了孔板纯化(plate-based purification)的玩法不可具备够了量的高纯净度免疫免疫免疫抗体样机大力支持后期的学习。从而,可以的发掘建设迅速的制法一些量高纯净度样机的措施,样机量约为10-100 mg成为“mid-scale”,可够了使用在生殖细胞产品检测、体內疗效检测各类生物技术工具性学习等,初始筛分出指标大碳原子结构。文章概述
内容报告范文好几回种抗原的科学规范纯化方试,分为Protein A亲和驯服结合体型大小排阻精心制作油的纯化环节制作高饱和度抗原样件。体型大小排阻脱离首选琼脂糖机质Superdex 200及硅胶制品机质的SRT-10C SEC-300二款商品确定赛果析,表明商品基本特性,首选为宜的流动的速度经济条件确定工作,获取但是(表1)信息显示赛分高新科技SRT-10C SEC-300含有较高的脱离度,精心制作油的抗原样件含有挺高的回收率和一定的饱和度,流动的速度可达到7.5 mL/min,且含有快一点的脱离的速度,非常大的情况上减掉生产研发时刻。进而,二、步抗原精心制作油首选SRT-10C SEC-300制作柱。 表1 SRT-10C SEC-300与Superdex 200纯化作用价格对比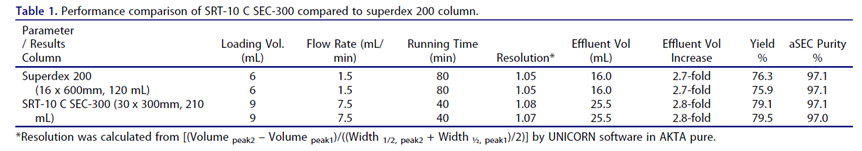

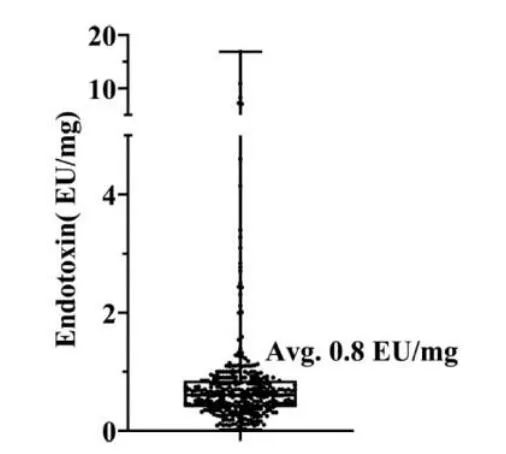
延展阅读
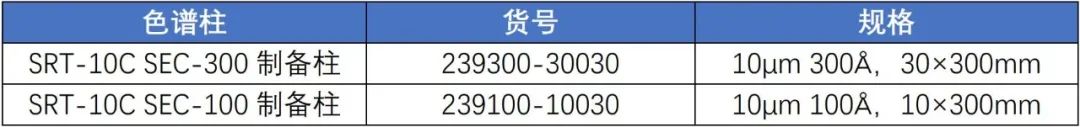
曾多次资料快运频道,简介SRT-10C体型大小排阻色谱食品还可运用于nm表面抗原的纯化。杏彩体育网 有限公司持续买家苏黎世社会和Linkster Therapeutics联手在《自然的》杂志期刊子刊《Nature Protocols》上发过的篇文章中提及SRT-10C SEC-100化学合成柱运用于nm表面抗原的纯化,有没有效调低色谱峰拖尾毛病,挺高纯化使用效果。 [1] Xiaomin Yang, Richard Yuan, Christopher Garcia, Jessica Berry, Denisa Foster, Dongmei He, Gui-Feng Zhang & Bryan E. Jones (2021) Development of a robust and semi-automated two-step antibody purification process, mAbs, 13:1, 2000348, DOI:10.1080/19420862.2021.2000348订购信息




 留意赛分
留意赛分